实验 1 甲酸蒸气的二聚热
1 学习目标
完成本节实验并填写报告后,您应能够:
- 安全、高效地使用施伦克线(Schlenk line)处理气体和蒸气。
- 自信地使用傅里叶变换红外光谱仪(FTIR)和温控红外气体池来采集和处理蒸气的红外光谱。
- 从化合物的振动光谱中提取其热力学性质。
甲酸二聚体形成的热力学
羧酸分子即使在气相中也具有强烈的缔合作用。电子衍射研究²表明,甲酸蒸气中富含一种由两个氢键(虚线所示)稳定的平面二聚体形式,如图1所示。
 图 1 甲酸二聚体的结构
图 1 甲酸二聚体的结构
因此,甲酸的气相红外光谱表现为单体和二聚体吸收带重叠的混合光谱。在给定温度下,建立了二聚化平衡:
该平衡的特征在于二聚化平衡常数 ,其定义为
根据方程 2,由于二聚体的浓度随单体分压的平方呈二次方增加,总样品压力的变化将引起单体/二聚体比例的变化,从而可以通过适当的数据处理来分离重叠的单体和二聚体光谱。
随着温度升高,平衡(1)向左移动,有利于更高的单体浓度和更低的二聚体浓度。因此,如果单体和二聚体的特征能够被完全分辨,并且已知的比尔-朗伯定律积分吸收系数,就可以通过红外吸收光谱实验确定平衡混合物的组成和平衡常数的值。
在本实验所用的浓度下,我们假设蒸气组分表现为理想气体,即对于一摩尔蒸气,,并且比尔-朗伯定律为:,则:
其中: 吸收物质(二聚体或单体)的摩尔浓度 完全分辨的二聚体红外谱带的积分吸光度 完全分辨的单体谱带的积分吸光度 二聚体的积分消光系数 单体的积分消光系数 光程长度 R = 普适气体常数 随温度的变化取决于 的大小:
其中 分别是二聚化的标准自由能、焓和熵。对方程 4 进行重排并代入方程 3 可得:
使用方程(5)并知道吸收光谱的温度,我们可以计算出 ,即甲酸的二聚热。
2 实验步骤
第一部分 准备施伦克线
实用网站,最后访问日期:2025年9月10日 http://www.chemistryviews.org/details/education/3728881/Tips_and_Tricks_for_the_Lab_Air-Sensitive_Techniques_1.htmlํ http://www.ilpi.com/inorganic/glassware/vacline.html
 图 2. 施伦克线
图 2. 施伦克线
Step1
用双手操作,一只手握住活塞套筒,另一只手转动活塞芯,检查活塞 0、1、2 和 3 是否能轻松开关。如果不能,请清洁并用硅酮真空脂重新润滑。
Step2
施伦克线初始配置:
关闭的活塞:0、1、2 和 3 关闭的阀门:A、B、C、D、E 和 F 主冷阱和预冷阱处于室温
Step3
打开真空泵并打开活塞 0,当主冷阱被抽成真空时应能听到空气声。
如果管线没有泄漏,空气声应该会停止。
Step4
缓慢打开预冷阱的放气阀 B。等到空气声停止。
Step5
打开真空管线主阀门 C。等到空气声停止。
Step6
缓慢打开压力计阀门 D,同时观察 MicroLAB 压力传感器。避免突然打开阀门 D。
第二部分 红外气体池的抽真空与测试
Step1
将可变温度 10 厘米光程 NaCl 窗气体池(红外池)连接到设定为 的水循环器上。打开活塞 3,对连接气体池与施伦克线的管路进行抽真空。
Step2
关闭真空管线主阀门 C,并在三分钟内观察 MicroLAB(压力-时间曲线)。一个足够气密的系统在 5 分钟内压力应无变化。确保与 MicroLAB 528 接口的鲁尔锁连接牢固。
注意:不使用时,请将气体池保存在干燥器内。
Step3
如果没有泄漏,打开红外池阀门,对红外池抽真空约一分钟。在红外气体池阀门打开的情况下,关闭真空管线主阀门 C,并在 MicroLAB 上观察压力一分钟;压力应保持恒定。如果红外池无泄漏,关闭阀门 C 和通往气体池的活塞。
Step4
用一个杜瓦瓶浸没主冷阱和预冷阱,然后向杜瓦瓶中注入液氮(LN2)。
●安全风险:
缓慢加入液氮,以使杜瓦瓶在不过度飞溅的情况下达到 。
第三部分 向冷指管中填充甲酸
Step1
将 20 滴试剂级甲酸滴入球窝接头冷指管中。使用一个夹子,在冷指管和施伦克线之间连接一个凯氏(Kjeldahl)防溅球(图 2 中油鼓泡器旁的插图)。
Step2
将冷指管浸入一个杜瓦瓶中,加入液氮,然后将其连接到施伦克线上。打开活塞 2,在液氮浸没下对冷指管抽真空。您应该注意到 MicroLAB 图上的压力增加。
Step3
为对甲酸样品进行除气,执行三次冷冻-抽气-解冻循环。
Step4
打开通往气体池的阀门,通过打开活塞 3 再次对其进行抽真空。关闭真空管线主阀门 C,以 的分辨率,使用强切趾函数,采集 16 次扫描作为背景光谱。无需为每个温度采集不同的背景。
Step5
关闭通往施伦克线的主活塞 C,并确认系统无泄漏。将液氮杜瓦瓶从冷指管旁移开,让其升温。在此过程中,注意观察随着甲酸蒸气压在管线中增加,MicroLAB 上的压力也随之上升。
Step6
向气体池中采集约 0.015 atm 的甲酸蒸气。在多歧管上,关闭冷指管活塞 2 并将其浸入液氮中。
Step7
打开阀门 F 并缓慢打开 气体调节阀。
●安全风险:确保您看到油鼓泡器中有气泡冒出。
Step8
在鼓泡器中有良好气流的情况下,缓慢打开阀门 E,使红外气体池中的总压力达到 1 atm。
Step9
使用与背景相同的条件,进行 16 次扫描。
Step10
将样品稀释至原始浓度的 1/4(采集 0.2 Hg cm 的甲酸,并用 气体将总压力升至 1 atm)。
Step11
使用与背景相同的条件,进行 16 次扫描。
Step12
在最高至 的四个不同温度下再进行四次测量。实验结束时,您应共有十次测量:在每个温度下,都有一张高压光谱和一张低压光谱。存储这些光谱以备后续数据处理。
3 数据处理
Step1
您在 下的光谱必须看起来像下面的示例:
 图 3. 甲酸蒸气在 和 0.01 atm 下的光谱
KBr 窗口,10 cm 光程。注意光谱范围: 到
数据采集:16 次扫描,强切趾,分辨率
图 3. 甲酸蒸气在 和 0.01 atm 下的光谱
KBr 窗口,10 cm 光程。注意光谱范围: 到
数据采集:16 次扫描,强切趾,分辨率
Step2
对于每个温度,展开在两种不同压力下采集的光谱,如图 4 所示。
图 4 显示了在 和 0.01 atm 下采集的甲酸蒸气光谱中, 处单体峰下的面积。使用 OMNIC 软件,按照计算文件中的建议,计算单体和二聚体峰下的面积。
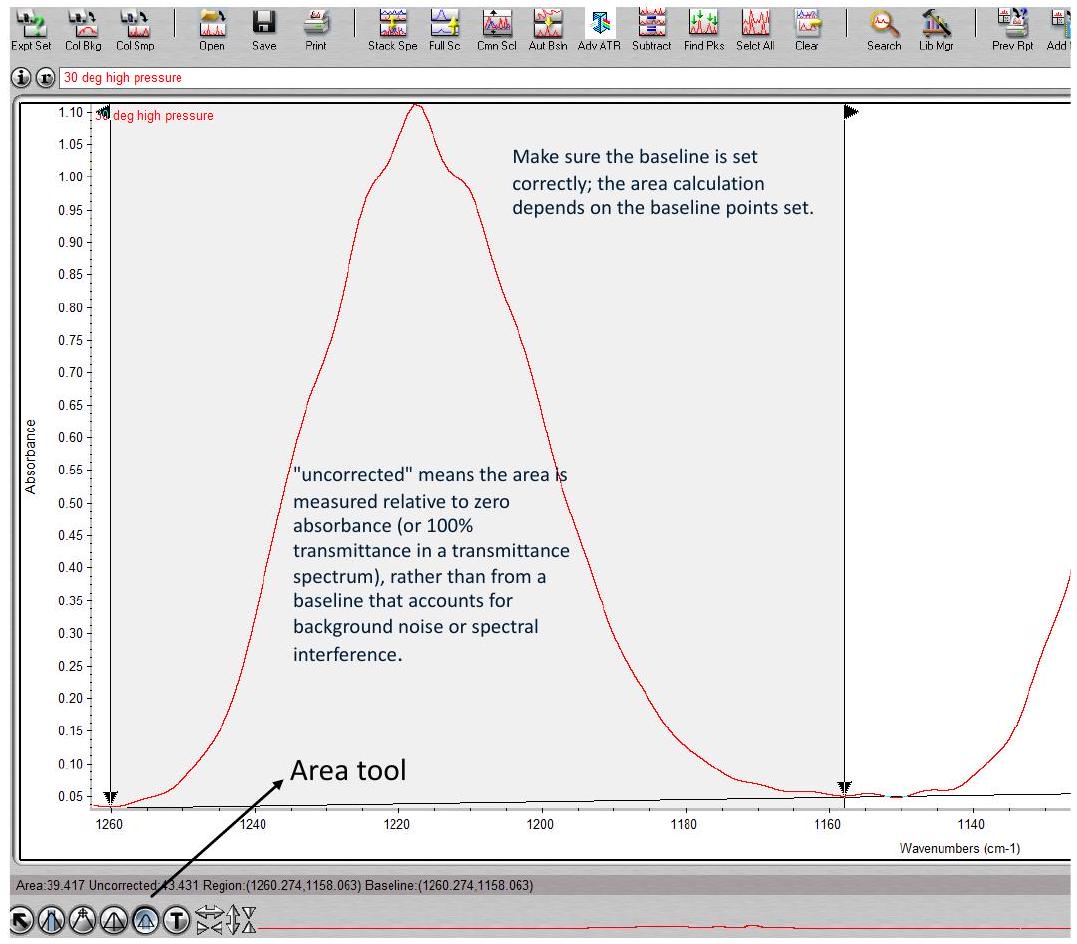
Step3
对稀释和浓缩样品,分别在 (二聚体)和 (单体)处的吸收带进行积分(计算面积)。
参考文献
(1) G. Henderson, J. Chem. Ed. 64, 88 (1987). (2) J. Karl and L. Brockway, J. Am. Chem. Soc. 66, 574 (1944).